抗衰老機制一直是生命科學前沿熱點問題�,這個問題在人類和陸生模式生物中已進行了較為深入廣泛的研究���,但是鮮有關于海洋無脊椎動物壽命決定機制的研究報道�。紫扇貝和海灣扇貝同為Argopecten屬扇貝�����,但在長期進化的過程中演化出截然不同的壽命����。海灣扇貝的壽命一般不超過14個月���,而紫扇貝的壽命可長達7-10年�����,海灣扇貝與紫扇貝的種間雜交一代壽命比海灣扇貝顯著延長��,且表現出極其顯著的生長優勢�,因此紫扇貝和海灣扇貝是研究自然條件下海洋動物壽命決定機制的理想模型��。中國科學院煙臺海岸帶研究所王春德研究團隊利用生物信息學和分子生物學技術開展系統研究����,首次揭示了IIS通路核心基因的遺傳變異在兩種扇貝壽命決定中的重要作用�。相關研究成果分別發表于Aquaculture和Frontiers in Physiology��。
胰島素/IGF-1信號(IIS)通路是陸生模式生物調控其衰老和壽命的保守途徑����,其中FoxO和PTEN作為重要調節器在該通路中起著關鍵的調控作用�。團隊利用前期完成的紫扇貝和海灣扇貝的高質量基因組��,通過生物信息學分析發現FoxO和PTEN在進化過程中受到了選擇����,PTEN的特征基序HCxxGxxR鄰近位點和FoxO蛋白鄰近AKT磷酸化位點的氨基酸發生了變異�。此外���,兩種扇貝的FoxO在轉錄激活結構域附近發生了變異�����,可能會導致不同的FoxO轉錄活性���。因此���,推測這些關鍵位點的變異可能導致FoxO和PTEN活性的改變�。在陸生模式生物中�,營養限制可導致IIS通路活性被抑制�,提高FoxO和PTEN的活性��,從而延長壽命����。團隊發現��,營養限制導致兩種扇貝的FoxO和PTEN表達均顯著上調����,但海灣扇貝對營養限制響應速度更快�����、幅度更大��。電離輻射刺激后�����,紫扇貝的死亡率顯著低于海灣扇貝���,表現出更強的抗損傷和修復能力�����。輻照后FoxO的表達量在紫扇貝閉殼肌中顯著升高��,而在海灣扇貝中顯著降低��;PTEN的表達量在紫扇貝閉殼肌中顯著升高��,而在海灣扇貝中則無顯著變化�。敲降FoxO和PTEN基因的表達后����,抗氧化酶SOD和CAT基因的表達量顯著降低�����,同時老化標志酶 -半乳糖苷酶活性顯著升高��。這些研究結果表明��,IIS通路的核心基因FoxO和PTEN可通過營養感受�、DNA損傷修復���、抗氧化等作用實現代謝保護����、基因組穩定性維持以及有害自由基消除���,從而證明IIS通路關鍵基因的遺傳變異在海灣扇貝和紫扇貝的壽命決定中發揮重要作用����。研究結果將為動物壽命決定機制的研究提供新思路�,提升對動物衰老和壽命決定機制理論的認知����,同時可為培育長壽命雜交扇貝提供理論基礎����,具有較高的理論意義和應用價值���。
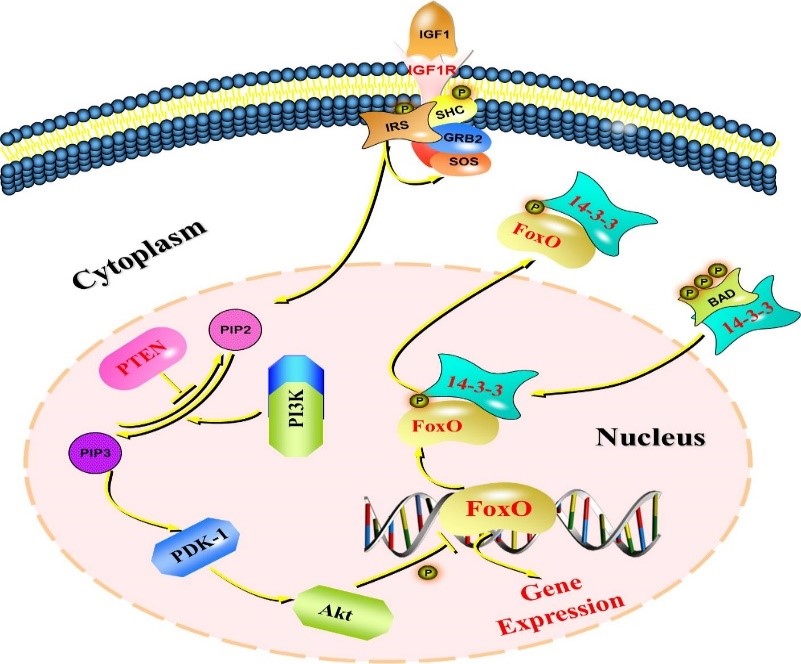
圖1. FoxO和PTEN參與衰老和壽命調控的IIS通路
本研究獲得國家自然科學基金�����、山東省農業良種工程項目����、山東省貝類產業技術體系和煙臺市科技計劃項目的支持��。中國科學院煙臺海岸帶研究所王媛(博士研究生)和許瀚之分別為兩篇論文的第一作者���,盧霞副研究員為兩篇論文的通訊作者�����。
論文信息:Yuan Wang, Xia Lu*, Chunde Wang, Junhao Ning, Min Chen, Ke Yuan, 2022. Potential roles of FoxO in promoting longevity in larger Argopecten scallops. Aquaculture, 561: 738690. DOI: 10.1016/j.aquaculture.2022.738690.
Hanzhi Xu, Xia Lu *, Chunde Wang, Junhao Ning, Min Chen, Yuan Wang, Ke Yuan, 2022. Potential roles of PTEN on longevity in two closely related Argopecten scallops with distinct lifespans. Frontiers in Physiology, 1386. DOI: 10.3389/fphys.2022.872562
論文鏈接:
